Perowskit-Kristalle speichern jetzt doppelt so viel Wasserstoff
Forschende erhöhen die Wasserstoff-Speicherkapazität von Perowskit auf 34 %. Das erleichtert Ammoniakproduktion und Energienutzung.

Perowskit-Kristalle wie dieses Gestein liefern die Vorlage für Materialien, die Energie und Ammoniakproduktion nachhaltiger machen.
Foto: Smarterpix / vvoennyy
Wasserstoff spielt eine wachsende Rolle in der Energiewende. Er gilt als vielseitiger Energieträger, kann aber auch Basis für andere Produkte sein. Besonders wichtig ist Ammoniak. Die Verbindung aus Stickstoff und Wasserstoff dient nicht nur als Grundstoff für Düngemittel, sondern auch als Speicherform von Energie. Forschende suchen deshalb Wege, Wasserstoff effizient zu speichern und ihn mit möglichst wenig Energieaufwand wieder nutzbar zu machen.
Gerade haben Forschende aus Japan die Wasserstoff-Speicherkapazität von Perowskit verdoppelt. Es wurde dafür zu Pulver zermahlen. Auch Metallpulver wird als Wasserstoffspeicher erforscht, zum Beispiel an der Ruhr-Universität in Bochum. Auch dort schauen wir kurz vorbei. Beide Materialien könnten die Wasserstoffwirtschaft entscheidend voranbringen – mit Folgen für Landwirtschaft, Industrie und Energietechnik.
Inhaltsverzeichnis
Perowskite: Kristalle mit großem Potenzial
Perowskit ist ursprünglich der Name eines Minerals, das im 19. Jahrhundert im Ural entdeckt wurde. Chemisch handelt es sich um Calciumtitanat (CaTiO3). Mittlerweile hat sich der Begriff jedoch verallgemeinert. Als Perowskit bezeichnet man heute viele Materialien mit einer bestimmten Kristallstruktur, die technisch interessant ist.
Diese Kristalle können nicht nur Strom leiten, sondern auch Wasserstoff einlagern. Forschende am RIKEN Pioneering Research Institute in Japan haben dafür eine neue Methode entwickelt. Der Leiter des Teams, Genki Kobayashi, erklärt: „Dieser Fortschritt ist eine gute Nachricht für die ökologische Nachhaltigkeit und wird uns letztendlich helfen, eine echte Wasserstoffwirtschaft zu erreichen.“
Japanische Forschung: Mehr Wasserstoff im Kristall
Am RIKEN-Institut verfolgt das Team um Genki Kobayashi einen ungewöhnlichen Ansatz. Statt wie bisher auf hohe Temperaturen oder großen Druck zu setzen, nutzen die Forschenden die Kraft der Mechanochemie. Dabei werden Stoffe durch starkes Mahlen und Mischen miteinander reagieren lassen.
Das Ziel: Wasserstoff möglichst tief in die Gitterstruktur von Perowskit-Kristallen einzubringen. Normalerweise sind dort Sauerstoffionen eingebaut. Werden diese durch Hydridionen ersetzt, entsteht Perowskit-Oxyhydrid. In dieser Form kann der Kristall Wasserstoff speichern und zusätzlich als Katalysator wirken.
Grenze fast verdoppelt
Bisher lag die Grenze bei etwa 17 %. Mehr Sauerstoff ließ sich nicht ersetzen. Das Team in Japan hat es geschafft, diese Grenze fast zu verdoppeln. „Langfristig erwartet man von unserem mechanochemischen Ansatz noch bessere Katalysatoren für die Ammoniaksynthese sowie Materialien für elektrochemische Geräte wie Brennstoffzellen“, so Kobayashi.
Die mechanochemische Herstellung bringt noch einen weiteren Vorteil: Sie verändert die Kristallstruktur so, dass die Katalysatorwirkung steigt. Selbst wenn die gleiche Menge Hydridionen eingelagert war, entstand bei den japanischen Tests mehr Ammoniak als bei den herkömmlich behandelten Pulvern. Der Mahlprozess versetzt das Kristallgitter quasi in eine vorteilhafte „Verformung“, die Hitze oder Druck nicht erzeugen können.
Das Forschungsteam stellte Bariumtitanat-Oxyhydrid sowohl mechanochemisch als auch mit herkömmlicher Hochtemperaturbehandlung her. Die Unterschiede waren deutlich: mehr Wasserstoff im Gitter, höhere Stabilität und eine bessere Ausbeute bei der Ammoniakproduktion. Kobayashi betont: „Kurzfristig liefern die neuen Erkenntnisse wertvolle Richtlinien für das Materialdesign.“
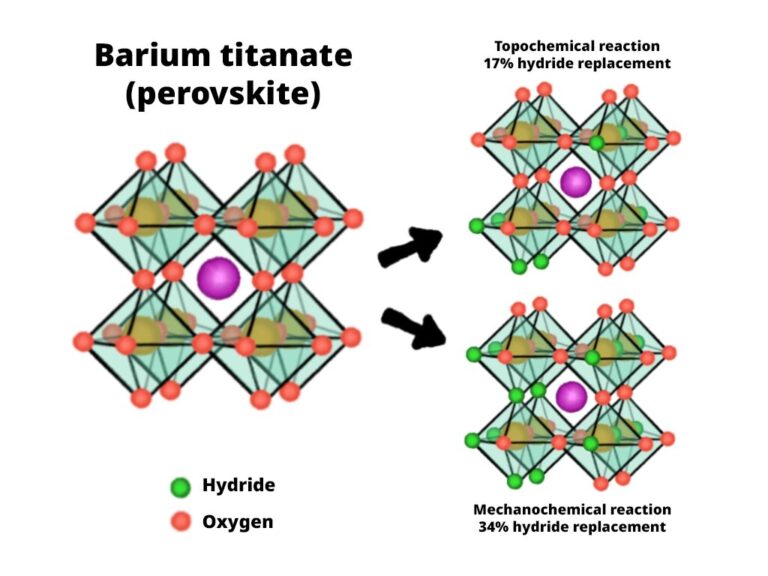
Bariumtitanat-Oxyhydrid wurde aus Bariumtitanat mittels standardmäßiger topochemischer Reaktionen (unter Anwendung von Wärme) und neuen mechanochemischen Reaktionen (durch Mahlen) hergestellt. Durch die mechanochemische Reaktion konnte die in Perowskit speicherbare Wasserstoffmenge von 17 % auf 34 % verdoppelt werden.
Foto: Riken
Mehr Wasserstoff speichern, mehr Ammoniak herstellen
Die Verdoppelung der Wasserstoff-Speicherkapazität hat gleich zwei Vorteile. Zum einen kann Wasserstoff in den Kristallen gespeichert und leichter transportiert werden. Zum anderen sind die so behandelten Perowskite bessere Katalysatoren für die Ammoniak-Synthese. Im Vergleich zu herkömmlichen Verfahren entsteht mehr Ammoniak, obwohl weniger Energie eingesetzt wird.
Warum ist das wichtig? Ammoniak ist die Grundlage für viele Düngemittel. Ohne ihn wäre die moderne Landwirtschaft kaum denkbar. Gleichzeitig kann Ammoniak auch als Energieträger eingesetzt werden. Er lässt sich lagern, transportieren und später wieder in Energie umwandeln. Ein Material, das diesen Prozess effizienter macht, hat damit eine doppelte Bedeutung: für die Ernährung der Welt und für die Energiewende.
Hier geht es zur Originalpublikation
Metallpulver als sichere Speicher
Neben Perowskiten verfolgen Forschende einen zweiten Ansatz: Metallpulver. Die Ruhr-Universität Bochum untersucht im Projekt „GreenH2Metals“ Legierungen, die Wasserstoff aufnehmen und wieder abgeben können.
Das Verfahren ist vergleichsweise einfach. Wasserstoffmoleküle treffen auf die Oberfläche der Partikel, werden in Atome gespalten und wandern ins Metallgitter. Dort bilden sie sogenannte Hydride. Senkt man den Druck, geben die Partikel den Wasserstoff wieder ab. Alles funktioniert bei Raumtemperatur und unter moderatem Druck.
Prof. Christian Liebscher vom Research Center Future Energy Materials and Systems erklärt: „Die bisher übliche Speicherung in Gas- oder Flüssigtanks hat verschiedene Nachteile.“ Dazu gehören hoher Energieaufwand und die Gefahr von Leckagen. Metallpulver dagegen speichern Wasserstoff sicher und nahezu verlustfrei. Sollte ein Tank beschädigt werden, tritt der Wasserstoff nur sehr langsam aus. Das Risiko einer Explosion sinkt deutlich.
Nachhaltigkeit durch Recycling
Ein weiterer Vorteil: Die Metalllegierungen können aus recycelten Rohstoffen hergestellt werden. Die Bochumer Arbeitsgruppe prüft, wie sich Verunreinigungen aus dem Recycling auf die Speichereigenschaften auswirken. Manche Fremdelemente könnten die Aufnahme von Wasserstoff sogar verbessern.
Mit modernen Mikroskopieverfahren wie der Atomsondentomografie untersuchen die Forschenden, wie sich die Materialien beim Be- und Entladen verhalten. Das Ziel ist klar: langlebige, effiziente und nachhaltige Speicher für grünen Wasserstoff.
Ein Beitrag von: