Warum Organe aus dem Biodrucker auf sich warten lassen
Gedruckte Organe aus dem 3D-Bioprinter? Der Beitrag zeigt, warum die Forschung boomt, aber es dennoch erst einmal Zukunftsmusik bleibt.
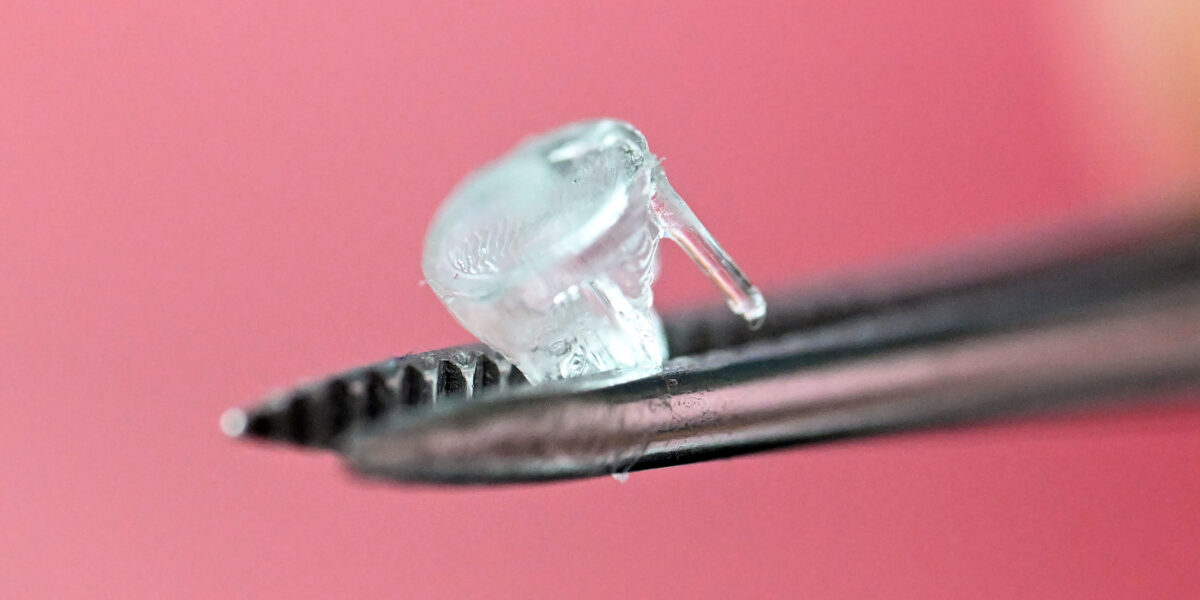
Beim Zentrum Health Technologies am Karlsruher Institut für Technologie (KIT) wird eine künstliche Baby-Herzklappe gezeigt, die in einem 3D-Drucker aus veganem Kollagen hergestellt wurde und derzeit dort entwickelt wird.
Foto: picture alliance/dpa | Uli Deck
Organe auf Knopfdruck bleiben vorerst Wunschdenken. Zwar hat das 3D-Bioprinting in der Medizin große Fortschritte gemacht, etwa bei Implantaten und Gewebemodellen. Doch bei funktionalen Organen wie Leber oder Herz stoßen Forschung und Technik an biologische Grenzen. Das Zusammenspiel mit dem menschlichen Körper bleibt schwer beherrschbar. Die Standardisierung und Regulierung hinkt hinterher. Auch wenn die Hoffnung groß ist: Geduld bleibt gefragt.
Selbst mit einer Pinzette lässt sich die winzige Herzklappe kaum greifen, die am Karlsruher Institut für Technologie (KIT) gedruckt wurde. „Eigentlich war das mal als Lippenfüller gedacht“, sagt Ute Schepers, Leiterin der Abteilung Chemische Biologie. Heute nutzen Forschende das Material für medizinische Anwendungen. Hergestellt wurde es von Bakterien, die Kollagen produzieren. Es könnte in Zukunft mit Zellen von Patientinnen und Patienten bestückt werden.
Das Verfahren nennt sich 3D-Bioprinting. Es basiert auf der Idee, lebendes Gewebe schichtweise zu drucken. Die Hoffnung: eines Tages Ersatzorgane zu produzieren, die individuell angepasst sind und problemlos transplantiert werden können. Doch diese Vision ist bisher nicht realitätsnah.
Inhaltsverzeichnis
- Vom Wunsch zur Wirklichkeit: Was Bioprinting kann
- Warum ein Organ mehr ist als ein Zellhaufen
- Standardisierung bleibt eine große Baustelle
- Erste Anwendungen bleiben Einzelfälle
- Mehr als Ersatz: Bioprinting im Labor
- Bioprinting für Tiere?
- Unklare Regeln und offene Fragen
- Forschung boomt, Geduld bleibt gefragt
- Medizinischer 3D-Druck: Schon jetzt im Einsatz
Vom Wunsch zur Wirklichkeit: Was Bioprinting kann
Die Grundidee des Bioprintings entstand vor rund zwei Jahrzehnten. Seither haben Forschende Methoden entwickelt, bei denen Zellmaterial zusammen mit stützenden Substanzen Schicht für Schicht zu Geweben geformt wird. Dabei kommen verschiedene Druckverfahren zum Einsatz. Beim sogenannten Inkjet-Verfahren werden winzige Tropfen von Biotinte über Druckköpfe auf ein Trägermaterial aufgebracht.
Was sich theoretisch einfach anhört, ist praktisch hochkomplex. Am KIT zum Beispiel wird an einer künstlichen Hornhaut geforscht. Ziel ist es, Patientinnen und Patienten mit Erkrankungen der Cornea passgenaue Lösungen zu bieten. Ein großer Vorteil: Die Zellen können vom jeweiligen Menschen selbst stammen. Damit sinkt das Risiko für Abstoßungsreaktionen.
Aus einer kleinen Hautprobe lassen sich Stammzellen erzeugen, die sich in andere Zelltypen umwandeln lassen. Daraus entsteht dann das gewünschte Gewebe. So weit die Theorie.
Warum ein Organ mehr ist als ein Zellhaufen
Doch der Druckvorgang ist nur der Anfang. Entscheidend ist, wie das gedruckte Gewebe im Körper funktioniert. „Nach einer Transplantation muss das Konstrukt in Wechselwirkung mit dem Organismus funktionieren“, sagt Niels Grabow von der Universitätsmedizin Rostock. Auf der einen Seite ist das Transplantat mit Blut in Kontakt, auf der anderen mit Gewebe. Die Anforderungen sind enorm.
Bei der Hornhaut funktioniert das besser, da sie nur zweidimensional aufgebaut ist. Je tiefer man aber in den Körper geht und je größer das Organ, desto schwieriger wird es. Die Leber wiegt rund ein Kilogramm und besteht aus vielen verschiedenen Zelltypen. Sie braucht zudem eine stabile Anbindung an Blutgefäße. „Da sprechen wir nicht mehr von einer dünnen Zellschicht.“
Standardisierung bleibt eine große Baustelle
Ein weiterer Stolperstein: der Mangel an Standardisierung. Materialien und Prozesse müssen so gestaltet sein, dass sie bei jedem Druckvorgang reproduzierbare Ergebnisse liefern. Erst kürzlich hat der Verein Deutscher Ingenieure (VDI) eine neue Richtlinie veröffentlicht. Sie soll helfen, Pilotprojekte auf eine gemeinsame Basis zu stellen.
Einheitliche Verfahren sind wichtig, wenn Bioprinting eines Tages in der Praxis ankommen soll. Bisher ist das aber nur in wenigen Fällen gelungen.
Erste Anwendungen bleiben Einzelfälle
Echte Einsatzbeispiele an Menschen gibt es bislang kaum. Die Hornhaut ist eine Ausnahme, weil sie äußerlich zugänglich bleibt. „Hier sind die Hürden vergleichsweise niedrig“, sagt Grabow. Die meisten Studien beschränken sich auf kleine Patientengruppen.
Gedruckte Ohrmuscheln oder Knorpel wurden bereits transplantiert, doch es handelt sich um Einzelfälle. Meist entstehen nur Teile von Geweben. Ganze Organe bleiben ein fernes Ziel.
Mehr als Ersatz: Bioprinting im Labor
Neben dem Ersatz können Bioprints auch als Forschungsmodelle dienen. Das Bundesgesundheitsministerium nennt die Untersuchung von Krebs als Beispiel. Gedruckte Gewebemodelle erlauben es, Wirkstoffe direkt auf realitätsnahen Zellstrukturen zu testen. Das könnte Tierversuche reduzieren oder ganz ersetzen.
Auch Schepers betont das Potenzial des „veganen“ Kollagens, das am KIT eingesetzt wird. Es sei eine vielversprechende Alternative zu tierischen Produkten.
Bioprinting für Tiere?
Nicht nur Menschen könnten profitieren. Auch für Tiere sind Anwendungen denkbar. „Haustiere haben ebenfalls Cornea-Probleme“, erklärt Grabow. Studien könnten sie einbeziehen. So ließe sich nicht nur forschen, sondern den Tieren auch direkt helfen. Ganz ohne zusätzliche Tierversuche.
Unklare Regeln und offene Fragen
Ein zentrales Problem: die regulatorische Unsicherheit. Woher dürfen die verwendeten Zellen stammen? Müssen sie vom Patienten selbst kommen? Sind Stammzellen erlaubt? Die EU arbeitet an Vorschriften, doch vieles ist noch unklar.
Auch Ausnahmeregelungen, etwa für Heilversuche bei austherapierten Menschen, stehen zur Diskussion. Die WHO sieht in der Kombination neuer biologischer und technischer Verfahren eine regulatorische Herausforderung.
Das Bundesgesundheitsministerium hingegen sieht aktuell keinen akuten Handlungsbedarf. Zu wenig ausgereift sei die Technik noch.
Forschung boomt, Geduld bleibt gefragt
Trotz aller offenen Fragen: Die Forschung entwickelt sich rasant. Laut Bundesforschungsministerium ist die Zahl der wissenschaftlichen Veröffentlichungen in den letzten zehn Jahren auf rund 1.000 pro Jahr gestiegen. Der neue Forschungszweig wird mittlerweile auch im Materialforschungsprogramm des Bundes berücksichtigt.
Grabow berichtet von einem regelrechten Ansturm auf Fördermittel. Selbst Projekte mit besten Bewertungen kämen nicht zum Zug. Auch Firmen investieren zunehmend in das Thema. Zahlreiche Patente wurden bereits angemeldet.
Medizinischer 3D-Druck: Schon jetzt im Einsatz
Während das Bioprinting für Organe noch in den Kinderschuhen steckt, zeigt der medizinische 3D-Druck in anderen Bereichen bereits Erfolge. Vor allem in Orthopädie und Zahnmedizin sind Implantate aus dem Drucker im Einsatz. Anders als beim Bioprinting enthalten sie kein lebendes Gewebe.
Verwendet werden Materialien wie Titan, Kunststoffe oder Keramik. Gedruckte Implantate können genauer auf den Körper abgestimmt werden als vorgefertigte Standardmodelle. Bei Krebspatient*innen kommen sie zum Beispiel zum Einsatz, wenn Knochenteile entfernt wurden. Dazu zählen Wirbelsäulenimplantate, Schlüsselbeinersatz oder Kieferknochen aus Titanpulver.
Auch Zahnärzte nutzen den Drucker
In der Zahnmedizin ist der 3D-Druck fast schon Alltag. Prothesen und Kronen lassen sich materialsparend und passgenau fertigen. Mit Intraoralscannern werden Zahnabdrücke digital übermittelt, Fehlerquellen reduziert. Die Folge: weniger Aufwand, bessere Ergebnisse.
Günstige Prothesen, neue Chancen
Auch bei Arm- und Beinprothesen gibt es Fortschritte. Individuelle Modelle aus dem 3D-Drucker sind deutlich günstiger als klassische Varianten. Während Letztere bis zu 35.000 Euro kosten, liegen die Druckversionen bei rund 800 Euro. Noch mit Abstrichen bei Haltbarkeit und Optik, aber mit großem Potenzial.
Ein weiteres Anwendungsfeld: Hörhilfen. Die Verbindung zwischen Ohr und Gerät, die sogenannte Otoplastik, wird zu 90 % im 3D-Druck gefertigt. Maßgeschneidert für die jeweilige Ohrmuschel. (mit dpa)
Weiterführende Informationen:
- https://www.vdi-nachrichten.com/technik/gesundheit/bioprinting-3d-druck-von-koerpereigenen-knorpelzellen-fuers-knie/
- https://www.vdi-nachrichten.com/technik/additive-fertigung/eis-koennte-das-bioprinting-revolutionieren/
- https://www.vdi-nachrichten.com/dossiers/biotechnologie/bioprinting-organe-aus-dem-3d-drucker/
- https://www.vdi-nachrichten.com/technik/gesundheit/bioprinting-der-kleinste-biodrucker-der-welt/
Ein Beitrag von:












