Robotische Minimotoren im smarten Implantat fördern Knochenheilung
Auf der Hannover-Messe 2026 zeigt ein Team der Universität Saarland den Prototyp eines smarten Implantats, in dem alles an Technik steckt, um die Heilung sichtbar zu machen und sogar aktiv zu fördern.

Auf der Hannover Messe zeigt das Team von Paul Motzki (l.) den Prototyp eines smarten Implantats - im Bild: Prof. Paul Motzki und Floria Wein. Foto Oliver Dietze
Foto: Oliver Dietze
Ab Tag eins der Operation sollen sie erkennen, ob ein Knochenbruch gut verheilt, und bei Bedarf gezielt nachhelfen: Implantate, die nicht nur den Knochen stabilisieren, sondern selbst etwas für seine Heilung tun, entwickelt an der Universität des Saarlandes ein Team aus Ingenieurwissenschaft, Medizin und Informatik. Wie die Universität mitteilt, liefert das Ingenieurteam um Paul Motzki dafür Mikroantriebe mit Formgedächtnistechnik samt Sensorik. Den medizinischen Part steuern Bergita Ganse und ihre Arbeitsgruppe bei.
Projekt Smarte Implantate: 8 Mio. Euro Förderung durch Werner-Siemens-Stiftung
Ob ein Knochenbruch verheilt, lässt sich bislang erst nach Wochen auf Röntgenbildern erkennen, heißt es weiter. Bis dahin bleibte die Heilung eine Blackbox. Genau an dieser Stelle setzen Forscherinnen und Forscher der Universität des Saarlandes an. Die Medizinerin Bergita Ganse ist Expertin für Frakturheilung.
Sie koordiniert an der Universität des Saarlandes das von der Werner-Siemens-Stiftung mit 8 Mio. Euro geförderte Projekt „Smarte Implantate“. Ziel sei es, maßgeschneiderte Implantate zu entwickeln, die künftig im Körper permanent kontrollieren und sichtbar machen, wie gut oder schlecht ein Bruch verheilt. Überdies sollen sich die Implantate dem Heilungsverlauf anpassen und sich versteifen, aber auch weicher werden und: Sie sollen die Knochenheilung sogar aktiv fördern durch gezielte Mikromassagen am Frakturspalt.
Antriebe mit Sensoreigenschaft am Knochenbruch
Paul Motzki und sein Team zeichnen den Angaben zufolge verantwortlich für die Technik, die in den Implantaten steckt. Sie sind Spezialisten für smarte Materialsysteme, also Materialien, die selbst Sensor- und Antriebsfunktionen mitbringen. Mehrere Prototypen für intelligente Frakturimplantate haben die Ingenieurinnen und Ingenieure zusammen mit der Arbeitsgruppe von Bergita Ganse inzwischen entwickelt, mehrere Patente sind daraus hervorgegangen, heißt es weiter.
„Dieser Heilungsverlauf lässt sich an Messwerten ablesen.“
Prof. Dr.-Ing. Paul Motzki, Professur Smarte Materialsysteme für innovative Produktion
Auf der diesjährigen Hannover-Messe zeigt das Team von Motzki einen Prototyp eines Implantats, in dem alles an Technik steckt, um die Heilung sichtbar zu machen und auch aktiv zu fördern: Es kann zum einen direkt an der Bruchstelle messen, ob sich neues Knochengewebe bildet. Das Implantat erkenne, ob die dabei für eine Heilung typischen Mini-Bewegungen am Bruchrand ablaufen.
„Die Steifigkeit im Knochenbruch steigt, wenn neues Gewebe wächst. Dieser Heilungsverlauf lässt sich an Messwerten ablesen“, erklärt Motzki. Auch ist an den Messdaten erkennbar, wenn eine Bewegung dem Bruch schadet, etwa, wenn der Patient das Bein zu stark belastet – wo die Belastungsgrenze liegt, kann dabei individuell eingestellt werden.

Zum anderen kann das Implantat sich durch einen patentierten Mechanismus aktiv am Bruch bewegen und sich dem Stadium der Heilung anpassen. Zu Beginn, wenn die Knochenstücke Halt brauchen, kann sich das Implantat versteifen und den Knochen fixieren. Im Laufe der Heilung kann es sich weicher schalten. Und: Es kann im Zusammenspiel von robotischen Minimotoren kleine Bewegungen in Form von Kontraktionen bis hin zu schnellen Vibrationen ausführen, um gezielt Wachstumsprozesse auszulösen.
„Die Heilung verläuft schneller, wenn der Bruchspalt gezielt bewegt und das Gewebe am Bruchrand stimuliert wird. Mit winzigen Bewegungen mit einem Hubweg etwa von 100 bis 500 Mikrometern lassen sich Wachstumsprozesse auslösen“, erläutert Medizinerin Bergita Ganse.
Formgedächtnisdrähte als Motor und Sensor zugleich
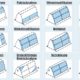
Hinter alldem stecken Bündel haarfeiner Nickel‑Titan‑Drähte, die in den Implantaten als Minimotoren und zugleich als Sensoren dienen, heißt es weiter. Sie können sich über dem Bruchspalt zusammenziehen oder auch mehr Spielraum geben. Möglich werde dies durch die besonderen Eigenschaften der Drahtbündel aus Nickel‑Titan, einer Formgedächtnislegierung.
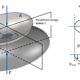
Nickel-Titan besitzt zwei Phasen. Das Kristallgitter der einen Phase ist kürzer als das der anderen. Werden die Drähte erwärmt, wechselt die Phase von einer in die andere. Fließt also Strom durch sie hindurch, erwärmen sich die Drähte, ihre Kristallstruktur wandelt sich um, und sie verkürzen sich. Nach dem Abkühlen bringen die Forscherinnen und Forscher die Drähte durch einen Mechanismus wieder in Ausgangsposition. Die besondere Eigenschaft der Phasenumwandlung im Kristallgitter nutzt Motzkis Team, um Bewegung ins Spiel zu bringen: Sie nutzen die Drähte als Antriebe.
„Nickel-Titan hat von allen Antriebsmechanismen die höchste bekannte Energiedichte.“
Paul Motzki
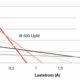
„Nickel-Titan hat von allen Antriebsmechanismen die höchste bekannte Energiedichte. Wir erreichen in sehr kleinen Dimensionen hohe Zugkraft“, erklärt Paul Motzki. Die Forscherinnen und Forscher bündeln mehrere Drähte, da diese im Bündel wegen der größeren Oberfläche schneller abkühlen. Hierdurch können sie schnelle Bewegungen mit hohen Frequenzen erzeugen. Sie können die Drähte steuern, weil das Material selbst bereits Sensoreigenschaften mitbringt: Da der elektrische Widerstand dieser Drähte sich verändert, sobald sie sich verformen, dienen sie den Forschern zugleich als Sensoren. Sie können jeder Verformung des Drahts einen präzisen Messwert des elektrischen Widerstands zuordnen.
„Mit diesen Messdaten haben wir neuronale Netze trainiert“, sagt Motzki. Anhand der Trainingsdaten lernen diese künstlichen Netze, Muster zu erkennen. „Auch bei Störeinflüssen arbeitet die KI zuverlässig“, erklärt der Ingenieurwissenschaftler, der an der Universität des Saarlandes und am Zentrum für Mechatronik und Automatisierungstechnik forscht, dessen wissenschaftlicher Geschäftsführer er ist.
Mit KI-Unterstützung: Implantat gibt Auskunft, ob der Knochenbruch heilt
Mithilfe der KI gibt das Implantat Auskunft, ob die Steifigkeit im Knochenbruch zunimmt – ohne dass Röntgenstrahlung zum Einsatz kommt. Die Rückschlüsse auf den Heilungsverlauf sind durch die Zusammenarbeit mit dem Team von Bergita Ganse möglich. Mittels der Messwerte lassen sich die Drähte präzise ansteuern und bewegen. Die Ingenieure können Bewegungsabläufe modellieren und programmieren, oder sie einfach in jeder beliebigen Stellung innehalten lassen. In der Praxis soll das Implantat die Informationen via Smartphone übermitteln und sich daüber auch steuern lassen, heißt es weiter.
Die Forscher miniaturisieren die Technik weiter, dabei werden sie auch von der EU im Programm Horizont Europa im Rahmen des 21-Millionen-Forschungsprojekts Smile (Smart implants for life enrichment) gefördert.
Hintergrund
- Das Saarbrücker Forschungsteam nutzt die Formgedächtnistechnik für die verschiedensten Anwendungen vom neuartigen Kühl- und Heizsystem bis hin zu Robotergreifern.
- An der Technik forschen auch zahlreiche Doktorandinnen und Doktoranden sowie Studierende mit.
- Sie ist Gegenstand zahlreicher auch international ausgezeichneter Veröffentlichungen in Fachzeitschriften und wird in mehreren großen Forschungsprojekten gefördert.
- Um die Ergebnisse der anwendungsorientierten Forschung in die Industriepraxis zu bringen haben die Forscher das Unternehmen mateligent GmbH gegründet, die ebenfalls am Saarland-Stand auf der Hannover-Messe vertreten sein wird.
(Quelle: Universtität des Saarlandes)