Nanoroboter lassen Knochenzellen wachsen
Winzige Roboter aktivieren Stammzellen, sodass aus diesen Knochenzellen entstehen. Klingt nach Utopie? Nicht für Forschende an der Technischen Universität München (TUM), denen dieser Durchbruch gelang. Mit der neuen Methode eröffnen sich ganz neue Chancen in der Medizin.

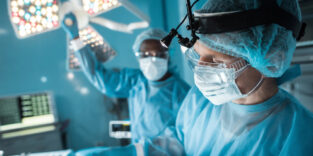
Chen Wang aus der Forschungsgruppe am Microbiotic Bioengineering Lab betrachtet das Ergebnis der erzeugten Knochenzelle.
Foto: Andreas Schmitz / TUM
Schnelle Heilungsprozesse bei möglichst wenig Nebenwirkungen – diesen Wunsch haben nicht nur zahlreiche betroffene Patientinnen und Patienten, sondern auch die behandelnden Medizinerinnen und Mediziner. Das Verfahren, dass Wissenschaftlerinnen und Wissenschaftler an der Technischen Universität München (TUM) gerade entwickelt haben, könnte genau diesen Wunsch erfüllen.
Sie haben einen Nanoroboter gebaut, der gezielt Stammzellen beeinflusst. Diese winzigen Maschinen üben fein dosierten Druck auf Zellwände aus, wodurch Stammzellen dazu gebracht werden, sich zuverlässig in Knochenzellen umzuwandeln. Das eröffnet neue therapeutische Anwendungen und beschleunigt Heilungsprozesse.
Besondere Struktur der innovativen Nanoroboter
Federführend bei der Entwicklung war Berna Özkale Edelmann, Professorin für Nano- und Mikrorobotik an der TUM. Im Microrobotic Bioengineering Lab arbeitet sie mit ihrer Forschungsgruppe interdisziplinär mit weiteren Instituten und Fachleuten der TUM an der Idee, die Biomedizin durch Nanoroboter entscheidend weiterzubringen.
Das Besondere an diesen Robotern: Sie sind aus mikroskopisch kleinen Goldstäbchen und flexiblen Polymerketten gemacht. In winzigen Gelkissen von nur 60 Mikrometern Durchmesser befinden sich Millionen dieser Partikel sowie einige menschliche Stammzellen. Durch den gezielten Einsatz eines Lasers werden die Roboter aktiviert und bewegen sich so, dass sie sanfte mechanische Reize auf die Zellen übertragen.
Gezielte Reize durch Nanoroboter lassen Knochenzellen wachsen
Das Team kann mithilfe von Laserlicht nicht nur die Bewegung präzise steuern. „Wir erhitzen das Gel lokal und können mir unserem System die Kräfte exakt bestimmen, mit denen die Nanoroboter auf die Zelle drücken – und sie so anregen“, erklärt Berna Özkale Edelmann.
Diese kontrollierten Belastungen aktivieren in den Stammzellen biochemische Reaktionen, die Signalproteine anregen. Darunter auch solche, die bei der Bildung von Knochengewebe eine zentrale Rolle spielen.
Trainingsprogramm für Stammzellen
Die Forschenden haben herausgefunden, dass schon ein schwaches, rhythmisch wiederkehrendes Druckmuster genügt, um Stammzellen innerhalb weniger Tage zu aktivieren. Das Ergebnis: In rund drei Wochen hatten sie stabile Knochenzellen vorliegen.
Laut Özkale Edelmann lassen sich ähnliche „Trainingsprogramme“ auch auf andere Zelltypen übertragen: „Das ist fast wie im Fitness-Center: Wir trainieren die Zellen für einen ganz spezielle Einsatzbereich. Jetzt müssen wir nur noch herausfinden, welches Belastungsmuster zum jeweiligen Zelltyp passt.“
Stammzellen als Basis für neue Knochenzellen
Ihr Ziel ist es, die beste Kombination aus Intensität und Frequenz des Reizes für verschiedene Zelltypen zu finden. So könnten künftig auch Knorpel- und Herzzellen mit ähnlicher Präzision herangezüchtet werden. Dadurch könnten regenerative Therapien deutlich beschleunigt werden.
Als Basis setzen die Forschenden dabei auf sogenannte mesenchymale Stammzellen. Sie gelten als vielseitige „Reparaturzellen“ des Körpers, weil sie das Potenzial besitzen, sich in verschiedene Zellarten wie Knochen-, Knorpel- oder Muskelzellen zu verwandeln. Diese Zellen sind nur wenige Mikrometer groß, bergen aber ein enormes regeneratives Potenzial, wenn sie präzise stimuliert werden.
Kontrollierte Mechanik: Knochenzellen wachsen dank Nanoroboter
Bislang stellte die gezielte Umwandlung in spezialisierte Zellformen Forschende vor große Herausforderungen. Mit dem neuen Ansatz gelingt es erstmals, Kräfte in einer dreidimensionalen Zellumgebung genau zu dosieren. Diese exakte Steuerung ist laut der TUM-Forscherin ein Durchbruch in der Nano- und Mikrorobotik, weil sie bisher in keinem anderen System vergleichbar umgesetzt wurde.
Das Team an der TUM hat mit dieser Methode einen Ansatz geschaffen, der weltweit einzigartig ist. Durch die gezielte mechanische Beeinflussung können biophysikalische Prozesse gezielt ausgelöst werden, die den Übergang von Stamm- zu Knochenzellen präzise steuern. Die Forschung liefert damit eine neue Grundlage, um auch andere Zelltypen planbar zu entwickeln.
Schnellere Produktion dank automatisierter Systeme
Die Entwicklung gilt als wichtiger Schritt für die regenerative Medizin, da sie kostbare Zeit in der Zellzüchtung spart. Statt unsicherer chemischer Stimuli nutzen die Forschenden mechanische Signale. Diese physikalische Präzision ermöglicht schnellere und reproduzierbare Ergebnisse – ein entscheidender Vorteil für spätere klinische Anwendungen.
Um den therapeutischen Bedarf zu decken, planen die Forschenden die Automatisierung der Zellproduktion. Für Anwendungen in der Medizin wären bis zu einer Million spezialisierter Zellen notwendig, erklärt Özkale Edelmann. Ein automatisiertes Verfahren könnte eine gleichbleibende Qualität sichern und die Zellmengen in kürzerer Zeit verfügbar machen.
Ein Beitrag von: